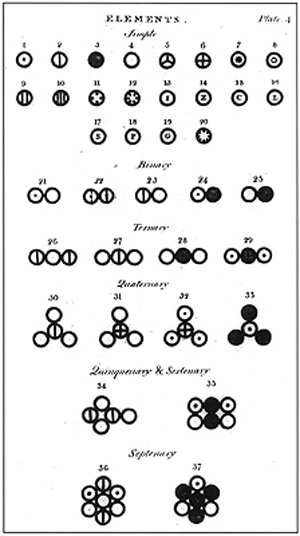
Modelo atómico
Desde el descubrimiento del átomo en los albores de la humanidad, gran cantidad de científicos y otros pensadores se han afanado en investigar y producir nuevos tipos de átomos, más potentes, limpios y rentables que los ya existentes. Dado el amplio mercado existente para esta mercancía, la investigación atómica ha experimentado una gran expansión en los últimos años, lo que ha llevado a la aparición de una gran cantidad de complejos modelos adaptados a todas las necesidades y bolsillos. En este artículo se analizarán detalladamente los engorrosos, pero principales modelos de átomos que han existido a lo largo de toda la historia de la humanidad y que han sido pieza fundamental para el desarrollo de las putas Matemáticas.
Modelo Dalton
Creados por los míticos pistoleros del Oeste Americano, los átomos Dalton experimentaron una gran popularidad durante los tiempos de la Fiebre del Oro a inicios del Siglo XIX, por su versatilidad y fácil manejo, ya que eran simples esferas que podían unirse y desunirse a voluntad. Esto los hacía idóneos para ser utilizados en condiciones precarias, como podía ser el interior de una carreta de bueyes o el lomo de un caballo. Pero su simplicidad también constituía su mayor defecto, ya que era extremadamente fácil perderlos y si se caían al suelo, llegaban a rodar largas distancias antes de desintegrarse espontáneamente.
Estos defectos hicieron que los átomos Dalton acabaran cayendo finalmente en desuso, siendo actualmente válidos solo como pieza de museo. Una reciente teoría especula sobre la participación de los átomos Dalton en el nacimiento del popular juego de las canicas, siendo ésta una versión que ha tomado particular fuerza en los últimos años.
Modelo Thomson
Algunos años después de la aparición del modelo Dalton, otro científico descubrió su secreto mejor guardado: los átomos no eran en realidad bolas macizas, sino que tenían dos partes, como un imán: una positiva y otra negativa. Dado que el modelo existente no permitía aprovechar ésta característica, especialmente útil para fijar notas a la nevera, Thomson desarrolló un modelo en el cual una esfera positiva tenía pegadas muchas pequeñas esferas negativas, como los trozos de chocolate de un pastel (se creía que Thomson estaba hambriento cuando desarrolló su teoría, pero hoy se sabe a ciencia cierta que era pastelero).
Este modelo gozó de un sorprendente, pero efímero, auge: aunque los átomos ya no rodaban, su ya mencionado parecido con un pastel causó innumerables ingestiones accidentales, con resultados que variaban desde la gastroenteritis leve hasta la implosión espontánea. Por este motivo, la fábrica recibió cuantiosas demandas, que obligaron a su cierre forzoso en el año 1904.
Modelo Rutherford
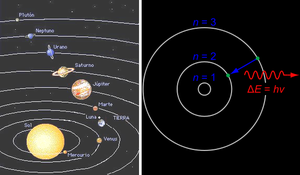
Tras el hundimiento de la fábrica de Thomson, siguió un periodo de oscuridad. El mercado del átomo se consideraba demasiado arriesgado y, en consecuencia, los inversores escaseaban, condenando la investigación atómica a un parón de varios años. No fue hasta 1911 que un relojero neozelandés, Ernest Rutherford, que en sus ratos libres investigaba el funcionamiento de los modelos de Dalton y Thomson, dio con la fórmula del éxito: una esfera maciza alrededor de la cual daban vueltas los electrones.
El modelo se hizo extremadamente famoso, ya que amén de un ensamblado mucho más sencillo, era el primer modelo atómico en movimiento. Su diseño estilizado y grandes prestaciones -para la época- popularizaron al átomo de Rutherford frente a los mucho más macizos y rudimentarios átomos de Dalton y Thomson. Hoy en día este modelo, aunque anticuado, sigue teniendo gran prestigio y se considera una nota de distinción en la decoración de escritorios, despachos y salones-comedor. Una versión más juvenil, el llamado Modelo de Bohr, se hizo popular por ser el primer átomo retratado en posters, camisetas, tazas y bolígrafos por todo el mundo.
Sin embargo, Rutherford apenas pudo disfrutar de su éxito: pocos años después de la salida de su modelo, se enfrentó a una demanda por plagio interpuesta por la familia de Galileo quienes afirmaban que el relojero había tomado la idea de su ilustre antecesor. Rutherford perdió el pleito y fue condenado a pagar una indemnización millonaria a la familia, lo que acabó llevándole a la ruina.
Modelo de Schrödinger
Fue creado en 1916 por un científico llamado Ervin Schrödinger. Se trata de un átomo de última tecnología, cuyos electrones no dan vueltas alrededor sino que se limitan a estar (o no) en una zona vagamente delimitada (o no) alrededor del núcleo. Aplicando aquí el principio que luego desarrollaría en su famoso gato, Schrödinger dice de su modelo:
Debido a su complejidad, este modelo no alcanzó mucha popularidad entre las masas. Sin embargo, sus peculiares características lo hacen el favorito entre los sabios despistados, que vieron en él la excusa perfecta para evitar las broncas de sus compañeros ("Si no sabes siquiera si está, ¿cómo sabes que lo he perdido yo?")
¿Sabía usted que...?
- Los primeros átomos de la historia estaban hechos de queso. Fueron desarrollados por un griego llamado Demócrito y dieron lugar a la peor plaga de ratones de la historia de la Grecia antigua. Pero como todo el mundo sabía, el mundo estaba hecho de aire, agua, tierra y fuego, por lo que su inventor no consiguió vender gran cosa.
- Durante la Edad Media el átomo fue ilegal en toda Europa y la posesión de uno solo de ellos se castigaba con la hoguera. El gran volumen de árboles que esto obligó a talar dio lugar a una de las peores crisis ecologistas de la historia, hasta la derogación de la ley en el siglo XVI por el Abate Molina.
![{\displaystyle \psi _{nlm}(\theta ,\phi ,r)={\sqrt {{\left({\frac {2}{na_{0}}}\right)}^{3}{\frac {(n-l-1)!}{2n[(n+l)!]}}2}}e^{-\rho /2}\rho ^{l}L_{n-l-1}^{2l+1}(\rho )\cdot Y_{l,m}(\theta ,\phi )}](https://wikimedia.org/api/rest_v1/media/math/render/svg/629eefffa63b5a5e05451d5b36e4975299deef73)